細胞內建的倒數計時器——端粒,它決定你老化的速度
你的每一個細胞裡,有一個正在倒數的計時器。
它不是比喻。它是一段真實存在的 DNA 序列,位於染色體的末端——叫做 端粒(Telomere)。
每次細胞分裂,這段序列就縮短一點。縮短到臨界長度,細胞就停止分裂,走向老化或凋亡。
這個機制,在 1980 年代被 Elizabeth Blackburn 和 Carol Greider 確認,並在2009年為她們帶來諾貝爾生理醫學獎。
但這個故事真正重要的部分,不是「端粒會縮短」——而是 縮短的速度,你有一定程度的控制權。
細胞為什麼不能無限分裂
二十世紀初,法國醫生亞歷克西.卡雷爾(Alexis Carrel)認為,只要環境與營養適當,細胞可以永遠生長繁殖——生命是可以無限延伸的。
這個想法在1960年代被推翻。科學家李奧納多.海佛烈克(Leonard Hayflick)與保羅.穆爾黑德(Paul Moorhead)用實驗證明:細胞分裂有其極限,大約複製 40 - 60 次之後就會進入休止期,不再繼續。
這就是著名的海佛烈克極限(Hayflick limit)。
對人體細胞而言,大約每 2.5 年更新一代,平均可複製分裂50代——據此推算,人類的理論壽命上限約為 125 歲。
但海佛烈克當時說不清楚:為什麼是 50 次?這個上限是什麼東西在控制的?
這個問題的答案,要等到端粒被發現才揭開。
端粒是什麼
染色體是細胞核裡存放遺傳訊息的結構。每條染色體的兩端,都有一段由重複序列組成的保護帽——這就是端粒。
人類的端粒重複序列是 TTAGGG,正常成年人的端粒長度約在 8,000–10,000 個鹼基對之間。
它的作用是:讓染色體在複製時,重要的遺傳訊息不會因為末端的磨損而遺失。每次細胞分裂,端粒犧牲自己的 25–200 個鹼基,保護了染色體上真正重要的內容。
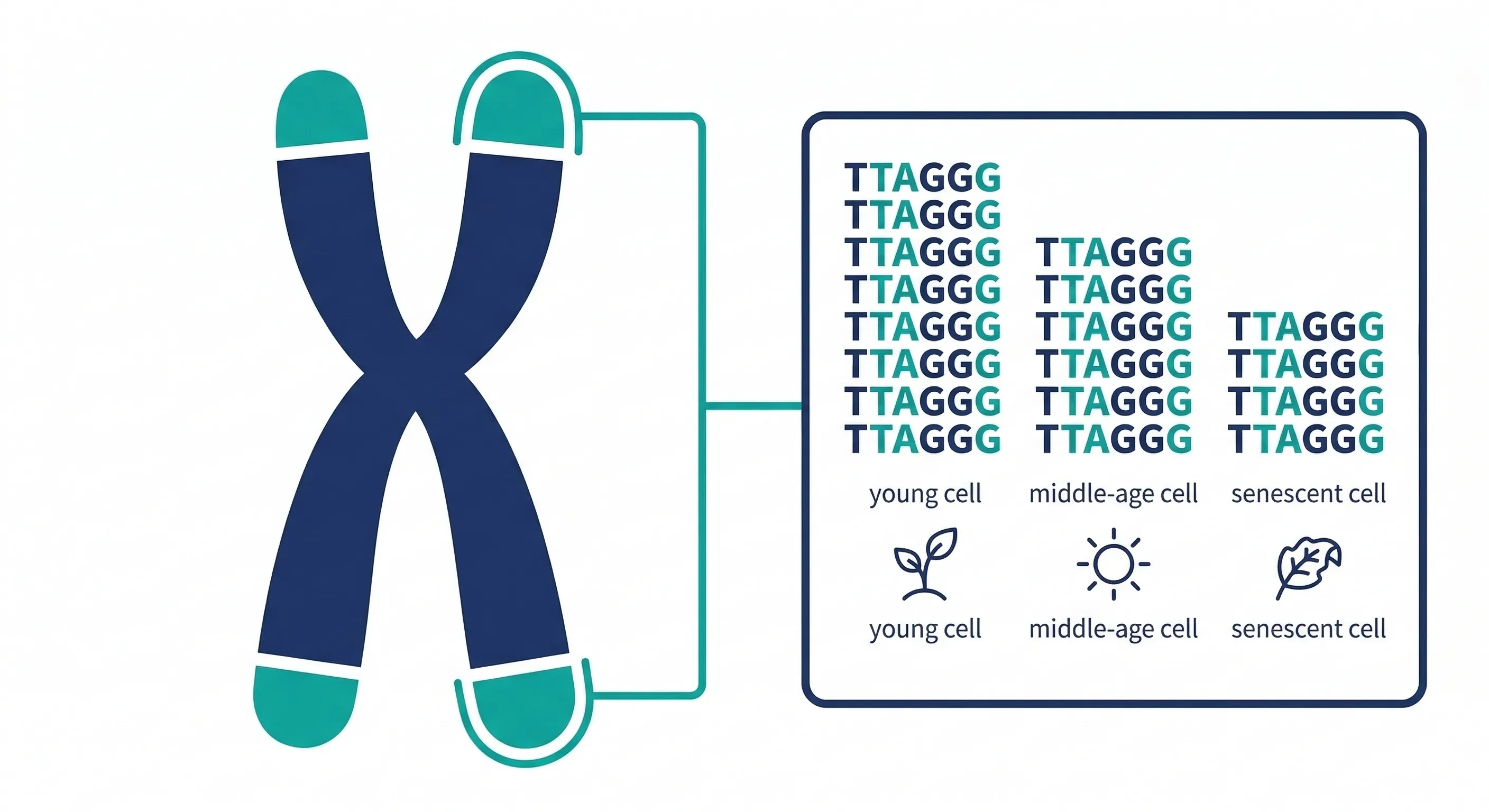
端粒縮短,和老化有什麼關係
當端粒短到一個臨界長度,細胞會啟動一個叫做 細胞衰老(Cellular Senescence)的程序——它不再分裂,但也不會立刻死亡。
這些衰老細胞會留在組織裡,持續分泌一組叫做 SASP(衰老相關分泌表型)的促發炎物質——細胞激素、蛋白酶、趨化因子。
這個訊號會做兩件事:
第一,招募免疫細胞——告訴身體「這裡有問題,需要處理」。這在正常情況下是好事,讓免疫系統清除受損細胞。
第二,擴散給鄰近細胞——SASP 的發炎訊號會讓周圍健康的細胞提前進入衰老狀態。一個衰老細胞,可以觸發周圍細胞的連鎖反應。
這就是端粒縮短和 Inflammaging(慢性低度發炎)的直接連結: 短端粒產生衰老細胞,衰老細胞分泌 SASP,SASP 製造更多慢性發炎,慢性發炎又加速端粒縮短。
這是一個自我強化的惡性循環。
什麼在加速端粒縮短
細胞分裂本身的磨損是不可避免的,但端粒縮短有快有慢——有些人 50 歲的端粒長度,相當於別人 70 歲的水準,反之亦然。
加速縮短的因素,目前研究最確定的有四個:
氧化壓力——自由基直接攻擊 DNA,而端粒富含鳥嘌呤(G),是氧化損傷最敏感的序列。氧化壓力高,端粒縮短速度顯著加快。這是慢性發炎和端粒之間最直接的攻擊路徑。
心理壓力——Elissa Epel 在 2004 年的研究(PNAS)中發現,長期照護病童的母親,端粒長度比同齡對照組短了相當於9–17年的老化量——壓力荷爾蒙皮質醇的長期升高,直接對端粒產生損傷。
睡眠不足——睡眠是細胞修復的主要時間窗口,慢性睡眠不足讓氧化損傷累積速度超過修復速度,端粒加速消耗。
慢性發炎(Inflammaging)——NF-κB 的持續活化增加 ROS(活性氧化物)產生,直接攻擊端粒序列。這形成了一個雙向的惡化循環:端粒縮短→更多 SASP→更多發炎→更多端粒損傷。
端粒長度,是目前最可量化的細胞老化指標之一
Richard Cawthon 在 2003 年的 Lancet 研究中追蹤了 143 名 60 歲以上的受試者,發現端粒較短的組,死亡率是端粒較長組的 3.18倍,其中心血管疾病死亡率高出 2.8倍,感染性疾病死亡率高出 8倍。
這是為什麼端粒長度被視為「生物年齡」的重要指標——它比日曆年齡更能反映你的細胞實際老化了多少。
但這裡有一個重要的區分要說清楚:
端粒長度和壽命之間,沒有簡單的線性關係。
老鼠的端粒長度是人類的 5 – 15 倍,但壽命只有 2 – 3 年。
靈長類的端粒長度比人類短,但壽命可以到 50 歲。
端粒長度的 縮短速度,比絕對長度更能預測老化速度。
這個縮短的速度,才是你應該關心的指標。
你能做什麼:減慢這個倒數
這裡要說清楚一件事:目前沒有任何口服補充品被嚴格科學驗證能有效延長端粒。
端粒酶促進劑的爭議、風險,以及消化系統這一關的根本限制,在另一篇說清楚了 →打爆保健品神話,以形補形為什麼不行?。
但減慢端粒縮短速度,有幾個方向是有可靠研究支持的:
降低氧化壓力——這是最直接的路徑。增加抗氧化物的攝取,特別是能進入細胞的脂溶性抗氧化物(類胡蘿蔔素、維生素E、CoQ10),減少自由基對端粒的直接攻擊。這也是 Prysm iO 皮膚類胡蘿蔔素掃描有意義的原因之一——它量測的,是你的抗氧化防禦水位,也就是你保護端粒的能力。
抑制慢性發炎(Inflammaging)——打斷端粒損傷和 SASP 的惡性循環,是同時保護端粒和減緩老化的核心策略。NF-κB 的抑制、Nrf2 的激活,都指向這個方向。
有氧運動——Denham 在 2016 年的統合分析(Sports Medicine)確認,規律有氧運動與端粒長度正相關。運動降低氧化壓力、提高粒線體效率、改善慢性發炎——三個路徑同時保護端粒。
睡眠品質——深層睡眠是細胞修復最集中的時間窗口,端粒的氧化損傷修復也在這裡發生。
壓力管理——皮質醇的長期升高對端粒的直接傷害,在研究中已有充分記錄。
這個倒數,你不能停止——但你可以減慢
端粒縮短是細胞生命的基本機制,沒辦法被「逆轉」。
但縮短的速度,取決於你的細胞環境——氧化壓力有多高、慢性發炎有多嚴重、修復機制是否正常運作。
這些都不是基因決定的,是你每天的細胞狀態在決定的。
延伸閱讀:
- 你的細胞儲備,正在被一個你感覺不到的過程悄悄耗光
- 抗慢性發炎就是在抗老化——這不是廣告詞,這是2000年就確立的科學
- 打爆保健品神話,以形補形為什麼不行?
- 平平都花一樣的錢,為什麼他有感但你沒感覺?
- 你的身體老化速度,有辦法知道嗎?——三種方法,從專業到居家
參考資料
- Carol W Greider, Elizabeth H Blackburn, 1985. Identification of a specific telomere terminal transferase activity in tetrahymena extracts. Cell. 43(2):405-413.
- Richard M Cawthon et al., 2003. Association between telomere length in blood and mortality in people aged 60 years or older. Lancet. 361(9355):393-5.
- Elissa S Epel et al., 2004. Accelerated telomere shortening in response to life stress. Proc Natl Acad Sci USA. 101(49):17312-5.
- Joshua Denham et al., 2016. Telomere Length Maintenance and Cardio-Metabolic Disease Prevention Through Exercise Training. Sports Med. 46(9):1213-1237.
- Judith Campisi, 2013. Aging, cellular senescence, and cancer. Annu Rev Physiol. 75:685-705.
- Vera Gorbunova et al., 2021. The role of retrotransposable elements in ageing and age-associated diseases. Nature. 596(7870):43-53.
- Kathryn Demanelis et al., 2020. Determinants of telomere length across human tissues. Science. 369(6509):eaaz6876.
先不要急著補,先看你現在屬於哪一型
如果你最近也有類似的情況,建議先做一個系統化的評估,看看你的身體警報目前在哪個水位。
⚡ 花 1 分鐘做身體警報風險評估評估結果是第一步。完成後,把結果和你的健檢數據一起帶進來,才能看出真正的方向。