你每晚都有一個清洗大腦的機會——但大多數人都錯過了
你每天晚上,都有一個清洗大腦的機會。
大多數人都錯過了。
不是因為沒有時間睡覺,而是因為睡了,但沒有真正進入大腦需要的那種睡眠。
大腦是人體唯一有「專屬清洗系統」的器官。
這套系統只在深度睡眠期間全速運作,負責沖走白天代謝產生的廢物蛋白,維護神經網路的正常運作。
如果這套系統長期無法好好工作,後果不只是「隔天精神差」那麼簡單——它與記憶退化、情緒失調、甚至阿茲海默症的早期病理都有直接關聯。
2019年,波士頓大學在《Science》期刊透過腦部影像,首次在人類身上看見這個過程:腦脊髓液像海浪一樣,在深度睡眠期間有節奏地沖洗整個大腦。
這篇研究讓「睡眠等於大腦清洗」從假說變成了可以被影像看見的事實。
以下,我們從運作機制、疾病關聯、到實際介入策略,完整解析這套夜間清洗系統。
類淋巴系統與神經流體動力學的生物物理基礎
大腦是人體代謝最旺盛的器官,雖然僅佔體重的 2%,卻消耗了約 20% 的能量。
這種高度的代謝活動必然產生大量的副產品,如β-澱粉樣蛋白(Amyloid-beta, Aβ)和 Tau 蛋白。
在身體其他部位,這些代謝廢物由淋巴系統回收;然而長期以來科學界一直找不到腦內代謝廢物是怎麼被清除的。
直到類淋巴系統的發現,才填補了這一學術空白。
類淋巴系統的運作架構
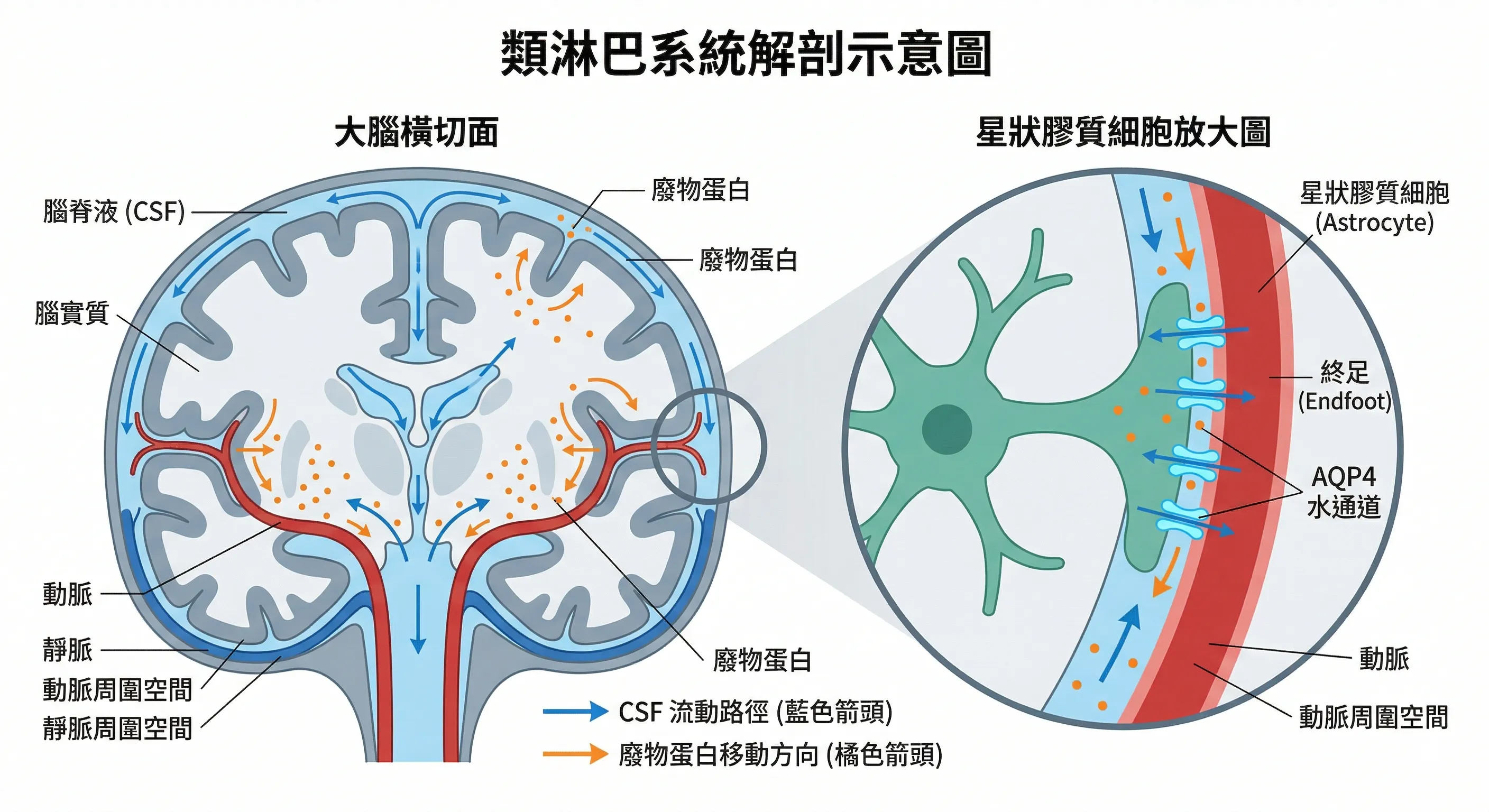
類淋巴系統是一個功能性的廢物清除路徑,其依賴於星狀膠質細胞及其末端足突上的水通道蛋白4(Aquaporin-4, AQP4)。
該系統的流動遵循特定的解剖路徑:腦脊髓液從蛛網膜下腔進入動脈周圍間隙(Perivascular Spaces,PVS),在 AQP4 的介導下,穿過組織間隙與組織間液(ISF)進行交換,最後將溶解的廢物帶向靜脈周圍間隙並排出腦外。
| 路徑組分 | 功能描述 | 生物物理關鍵因素 |
|---|---|---|
| 入口:動脈周圍間隙 (PVS) | CSF進入大腦實質的通道 | 動脈搏動產生的泵送動力 |
| 交換區:實質間隙 (Interstitial Space) | CSF與ISF的對流與擴散 | 間隙體積分數(α)與迂迴度(λ) |
| 出口:靜脈周圍間隙 | 廢物與流體離開大腦的路徑 | 匯流至頸部淋巴結進行體循環處理 |
 >
>
2019年《Science》論文的核心發現:巨觀波動的同步性
Fultz等人(2019)的研究展示了大腦清洗並非隨機的滲透,而是一場由神經活動引導的節奏性「海嘯」。
在非快速動眼期(Non-Rapid Eye Movements,NREM)睡眠中,大腦會出現頻率約為 0.05 Hz 的巨觀震盪。
這場「流體交響樂」的發生次序如下:
- 神經慢波出現:EEG紀錄到低頻、高振幅的慢波活動,代表大量神經元同步進入沉默狀態(Down states)。
- 血液體積縮減:由於神經活動減少,大腦對氧氣和葡萄糖的需求下降,導致大腦血流和血容量(BOLD訊號)減少。
- CSF脈衝流入:根據Monro-Kellie原理,大腦內部體積必須恆定。當血液體積退出時,壓力梯度驅動大量腦脊髓液湧入填補空間。
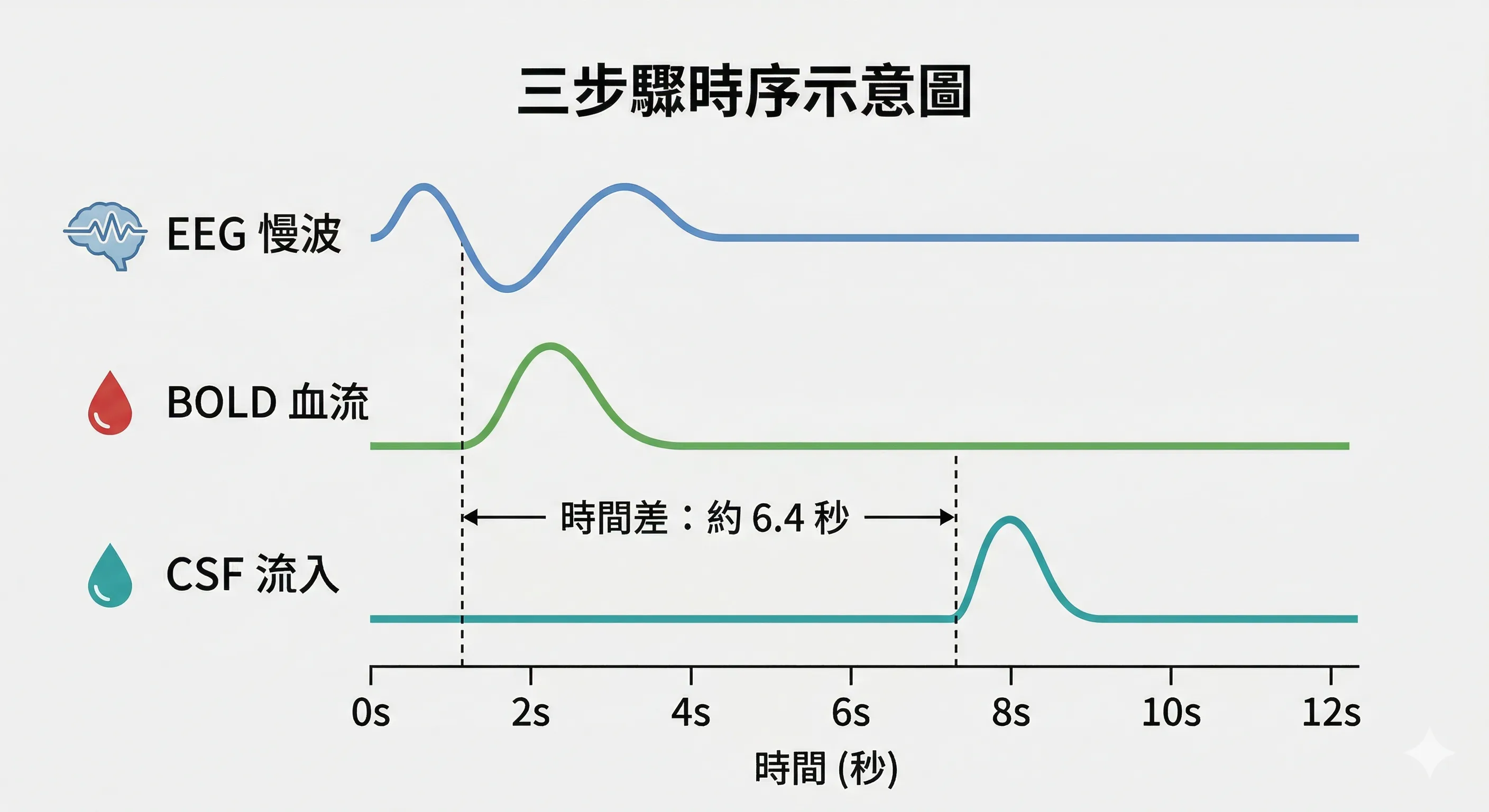
數據顯示,這種神經波領先於 CSF 波約 6.4秒。
這種精密的時序耦合確保了大腦在神經元休息的瞬間,獲得最大程度的物理清洗效率。
睡眠誘導的組織擴大與代謝清除效率
類淋巴系統最引人注目的特徵之一是它的「睡眠依賴性」。
研究表明,該系統在清醒狀態下幾乎處於關閉狀態,而在進入深度睡眠後,其清除效率可提高 十倍以上。
「60% 規則」:細胞間隙的動態擴張
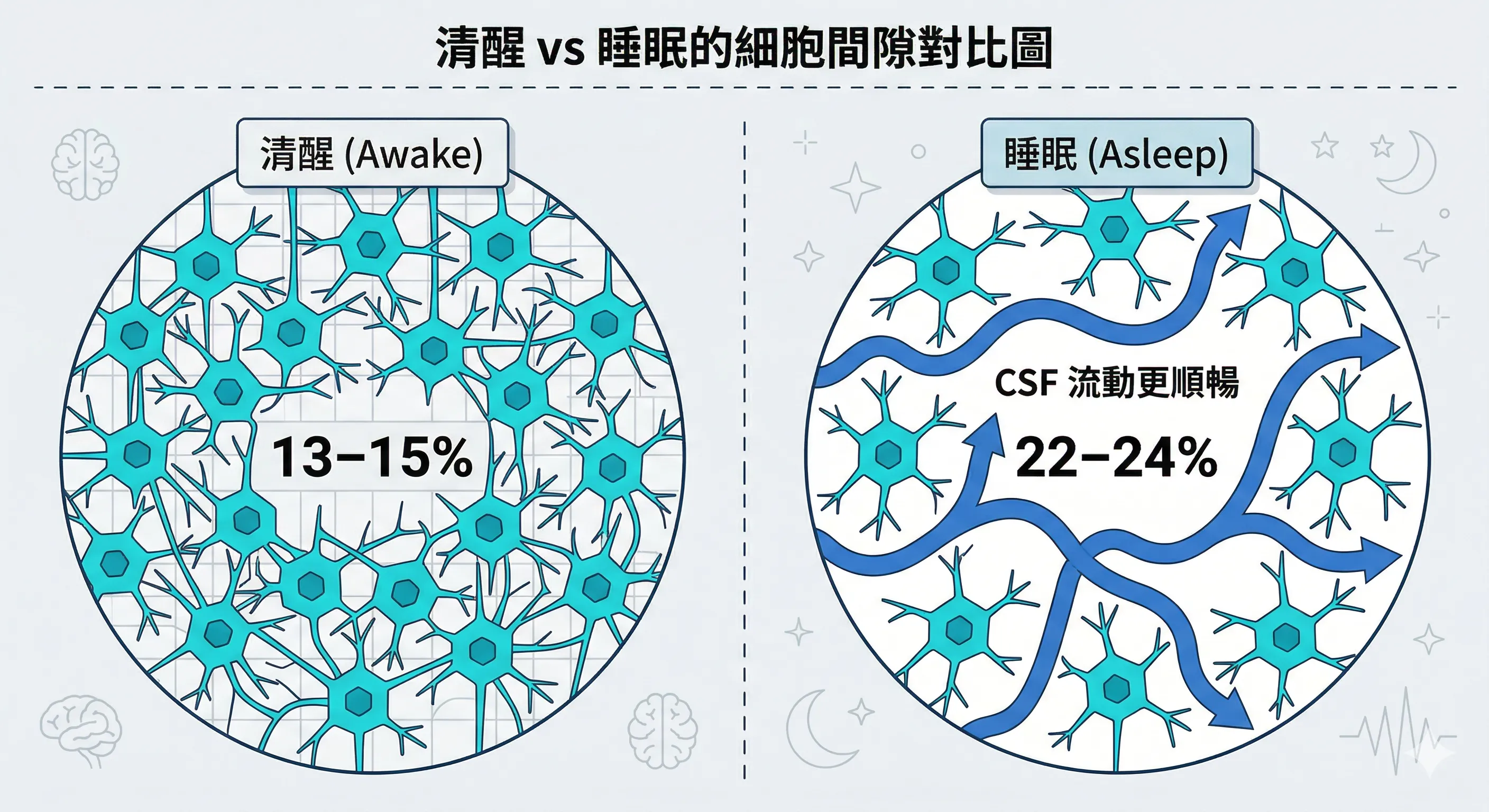
Xie等人(2013)在小鼠模型中發現,睡眠或麻醉會導致大腦細胞間隙的體積分數(α)增加約 60%。
在清醒狀態下,間隙空間僅佔大腦體積的13–15%;而在睡眠中,這一數值上升至 22–24%。
這種間隙擴張極大地降低了流體流動的阻力,使腦脊髓液能夠像「動力洗車」一樣沖刷神經元之間的空隙。
 >
>
去甲腎上腺素(Norepinephrine)的開關作用
調節這種間隙變化的分子開關是去甲腎上腺素。在清醒時,高水平的去甲腎上腺素會使神經元和膠質細胞體積保持膨脹。
當進入深眠後,腦幹中藍斑核(Locus Coeruleus)的放電頻率降至最低,去甲腎上腺素水平隨之下降,細胞收縮釋放出空間,成為類淋巴流動的高速公路。
睡眠剝奪的「複利損傷」效應
理解了類淋巴系統的運作機制之後,有一件事變得很清楚:睡眠不足的損害不是線性的,而是複利的。
每一個深眠不足的夜晚,廢物蛋白的清除效率下降,積累量增加。
第二天,起點就比昨天更髒一點。長期下來,這不只是疲勞問題,而是神經環境的持續惡化。
更關鍵的是:這種損傷並不只停留在「代謝廢物積累」這個層次。
最新研究顯示,睡眠不足會同時破壞大腦的 神經新生機制——也就是新神經元的生成能力——以及神經訊號傳遞所依賴的 分子修飾系統。
睡眠障礙與神經退化性疾病的惡性循環
長期睡眠不足是阿茲海默症與帕金森氏症的關鍵驅動因素,兩者具有顯著的雙向關係。
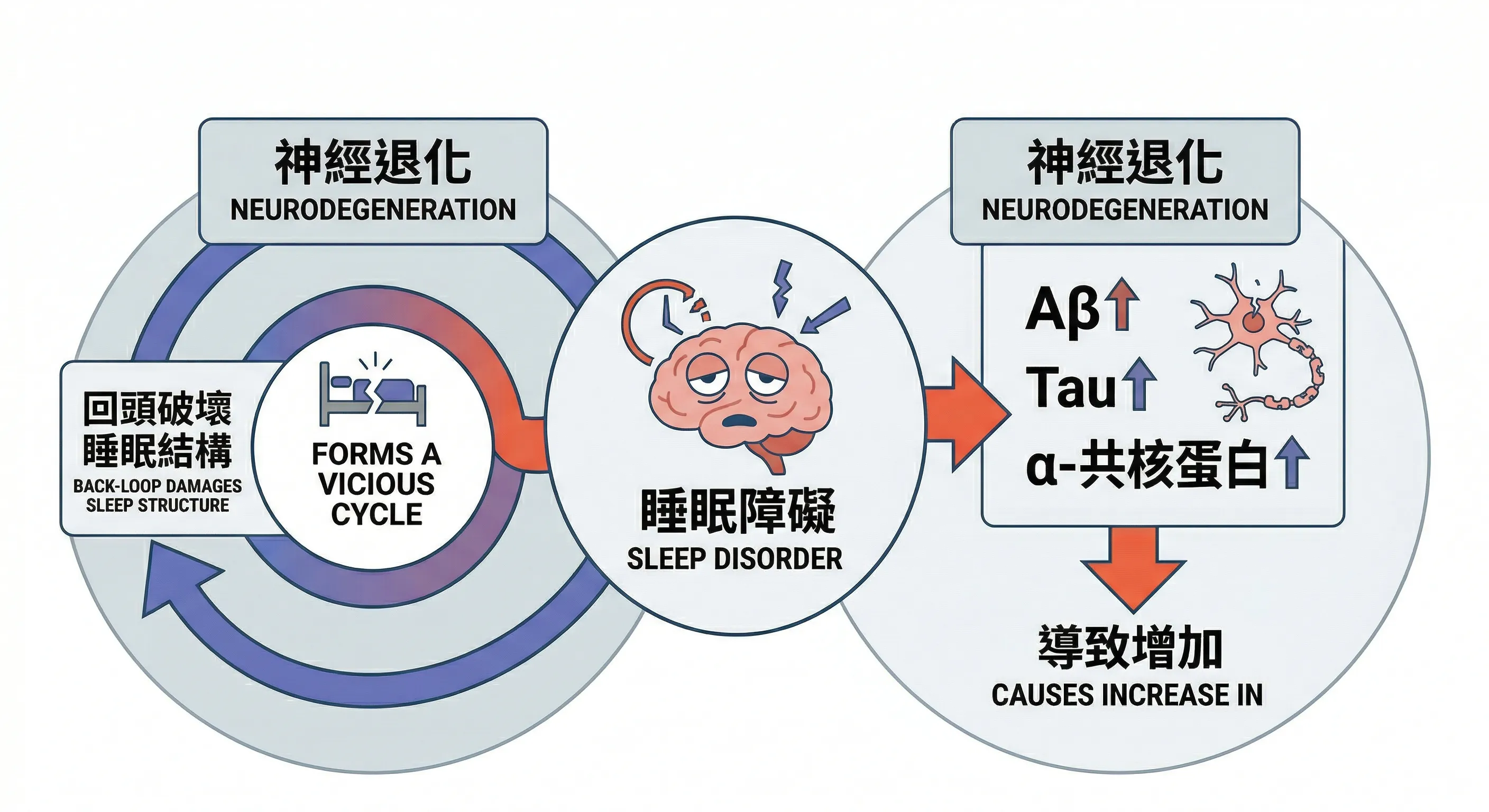
蛋白質病理積累
Aβ 的快速反應:僅一晚的睡眠剝奪就會導致人類大腦中 Aβ 水平升高約 25 – 30%。
Tau 蛋白的擴散:慢性睡眠不足會加速 Tau 蛋白在神經網絡中的傳播,積累與深度睡眠(Slow-Wave Sleep,SWS)的減少高度相關。
帕金森氏症與α-共核蛋白
類淋巴系統功能障礙導致α-共核蛋白無法有效清除,引發多巴胺神經元死亡。REM 睡眠行為障礙(Rapid Eye Movement (REM) Sleep Behavior Disorder,RBD)常被視為此類病變的前驅指標,可能早於運動症狀 11年 出現。
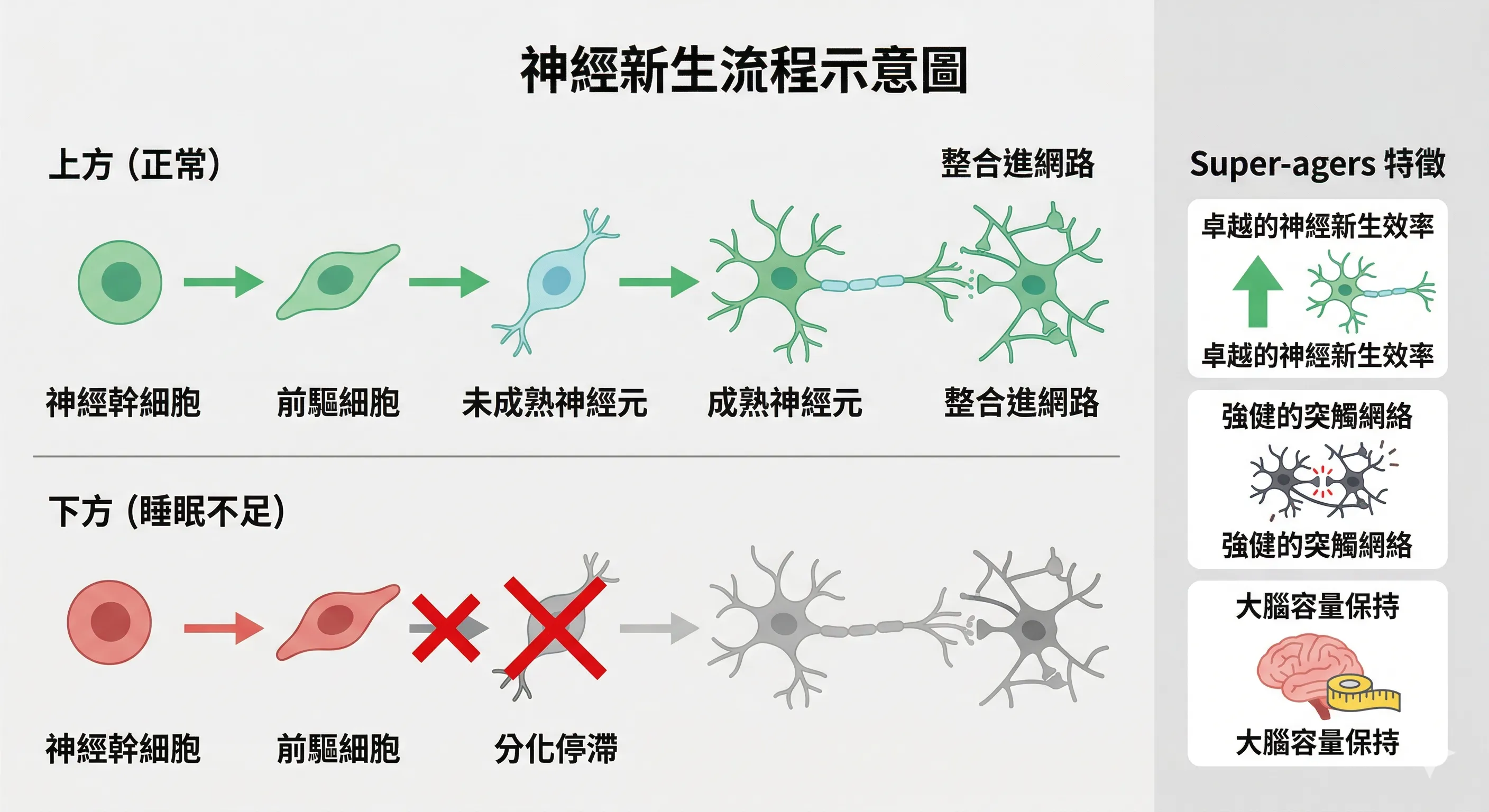
神經新生:睡眠不足正在關閉大腦的「自我更新」能力
阿茲海默症的神經退化,過去我們以為主要來自蛋白質積累(Aβ、Tau)。
2026年2月,《Nature》期刊一項分析 355,997 個人類大腦細胞核的研究,揭示了另一條更早開始的損傷路線:神經新生(Neurogenesis)的失調。
研究發現,在臨床前期阿茲海默症患者身上——也就是還沒有明顯失智症狀的人——海馬迴的神經幹細胞基因調控狀態就已經開始異常。
換句話說:大腦停止製造新神經元,早於記憶退化出現。
這對睡眠的意義是什麼?神經新生高度依賴睡眠品質:
睡眠不足 ↓ 皮質醇(壓力荷爾蒙)持續偏高 ↓ 海馬迴神經幹細胞受抑制 ↓ BDNF(神經滋養因子)活性下降 ↓ 新神經元生成減少、存活率下降 ↓ 海馬迴結構逐漸萎縮 ↓ 記憶與情緒調控功能衰退
同一項《Nature》研究也發現,80 歲以上但認知能力媲美 50 歲的「超級老年人(Super-agers)」,他們的共同特徵是:神經幹細胞活性接近年輕人,神經分化相關基因持續活躍,染色質維持開放狀態——大腦在分子層級保住了一個年輕的環境。而這套機制的維持,與睡眠品質密不可分。
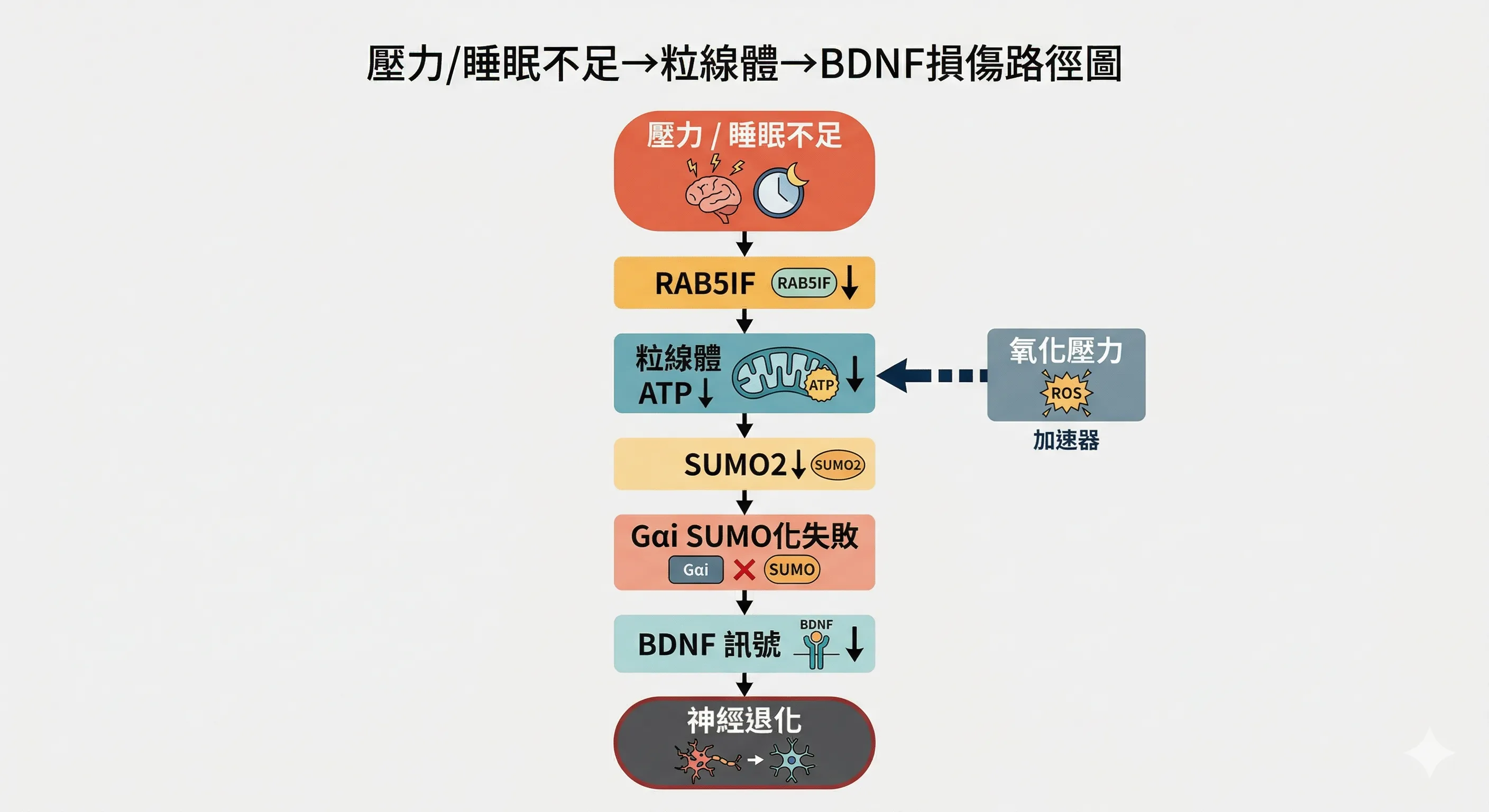
BDNF 訊號:壓力與睡眠不足如何從分子層級破壞大腦
神經新生需要一個關鍵分子來驅動:腦源性神經滋養因子(Brain-Derived Neurotrophic Factor,BDNF),也就是「大腦的養分」——它驅動神經幹細胞分化、維持突觸連結、保護神經元不退化。
2026年3月《Science Signaling》期刊揭示了慢性壓力破壞 BDNF 的具體分子路徑:
長期壓力 / 睡眠不足 ↓ RAB5IF 蛋白減少(粒線體調控蛋白) ↓ 粒線體 ATP 產量下降 ↓ SUMO2 合成不足(蛋白質修飾分子) ↓ G 蛋白 SUMO 化失敗(訊號轉導關鍵分子) ↓ BDNF-TrkB 訊號受阻 ↓ 神經突觸連結減少、神經新生下降 ↓ 情緒調控能力下降、出現憂鬱傾向
這條路徑有一個重要的起點:粒線體功能受損。
當睡眠不足導致氧化壓力增加、粒線體損傷加劇,整個路徑的每一個環節都同步惡化,形成惡性循環:
睡眠不足 → 氧化壓力↑ → 粒線體損傷 → ATP↓ → BDNF 訊號↓ → 神經退化↑ → 睡眠品質更差
也就是說:睡眠不足不只是讓大腦「沒洗乾淨」,它還在分子層級削弱大腦自我修復和更新的能力。
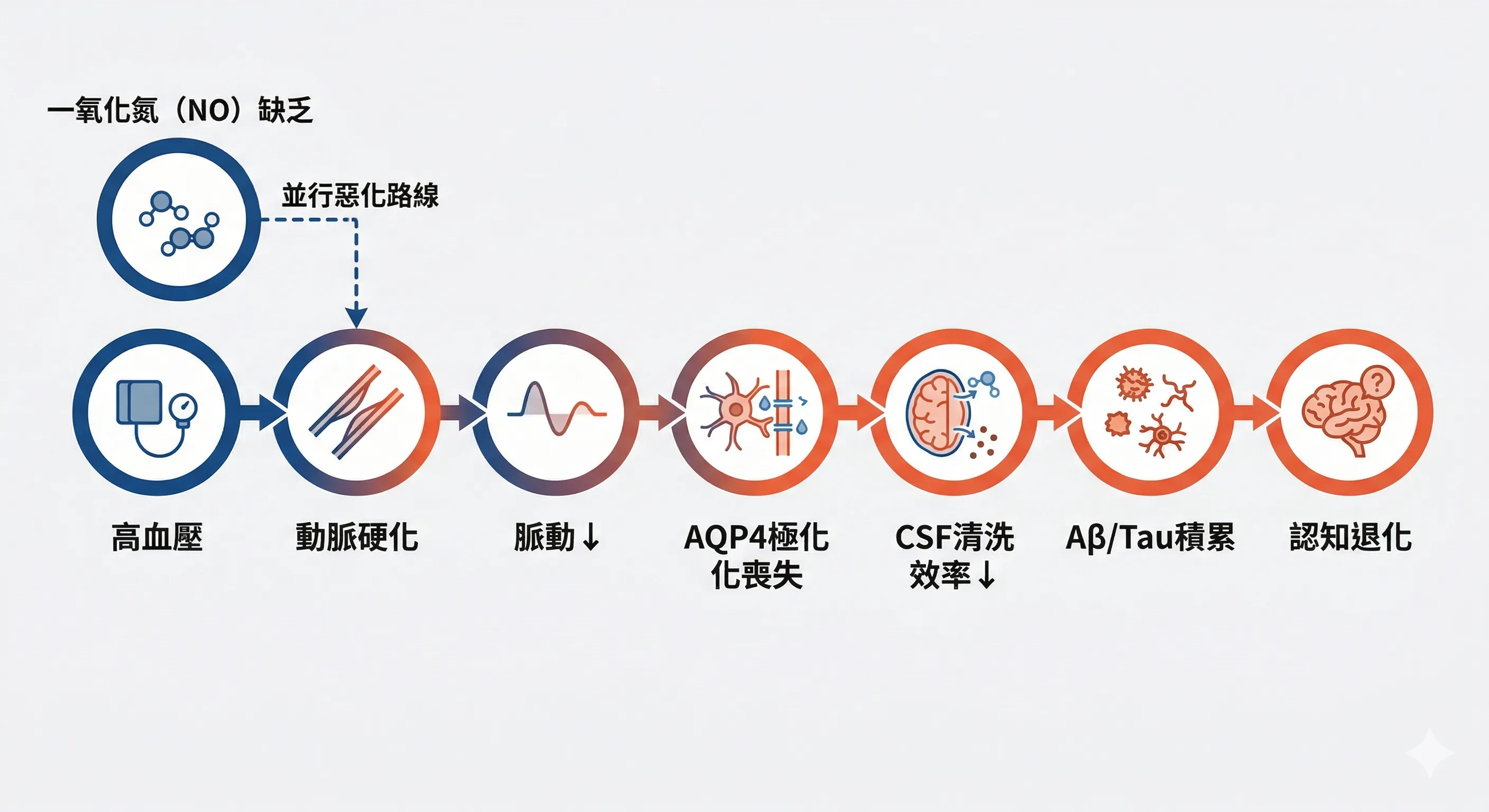
血壓:你從未想到的類淋巴系統殺手
大多數人知道高血壓傷心臟、傷血管。但很少人知道高血壓同時在悄悄關掉大腦的「清洗閥門」。
類淋巴系統的運作,高度依賴動脈脈動的物理推力。
每一次心跳,動脈壁的彈性收縮與舒張,會產生「蠕動泵」效應,把腦脊髓液沿血管周圍間隙向前推進。這個推力,是大腦清洗的主要引擎。
當高血壓長期存在,動脈壁逐漸硬化——平滑肌肥厚、膠原蛋白增生——血管失去彈性,脈動振幅減小。
研究已證實:誘導高血壓的動物模型中,腦脊髓液流速顯著減慢。
連鎖反應如下: 高血壓 ↓ 動脈硬化、脈動振幅下降 ↓ 類淋巴系統推進力不足 ↓ AQP4水通道極化喪失(星狀細胞失能) ↓ Aβ、Tau蛋白清除效率下降 ↓ 神經毒性蛋白持續積累 ↓ 認知功能退化
還有一條更細的路線:高血壓引發的慢性內皮損傷,會降低一氧化氮(NO)的生物利用度。
NO 不足讓血管更僵硬,同時破壞 AQP4 的正常排列——這個水通道蛋白負責讓腦脊髓液滲入腦組織,是清洗系統的「滲透閘門」。
兩個機制疊加,大腦的夜間清洗效率加倍惡化。
這解釋了一個長期被忽略的臨床現象:長期高血壓的人,即使從未發生中風,認知功能仍會提前退化。 不是腦血管「爆了」,而是大腦「洗不乾淨」。
血壓控制的意義,因此不只是保護心臟——而是保住大腦每晚進行清洗的物理條件。
神經病變年輕化趨勢與現代生活方式的衝擊
根據 2021 年全球疾病負擔(Global Burden of Disease,GBD)研究,早發型帕金森氏症(Early-Onset Parkinson’s Disease,EOPD)的全球發病率在過去三十年中增加了近 三倍。
現代年輕人晚間過度暴露於電子設備產生的短波藍光(460–480 nm),強烈抑制褪黑素分泌,進而壓縮深度睡眠比例。
這不只是「睡眠衛生」的問題。
藍光、晚間飲酒、不規律作息、慢性壓力——這四個因素都會從不同角度削減深眠比例,而深眠比例的下降,正是上述所有損傷路徑的共同起點。
營養學與植物營養素優化策略
特定的營養素已被證實能優化睡眠結構並提升大腦清洗效率:
蘇糖酸鎂與酸櫻桃汁
蘇糖酸鎂(Magnesium L-Threonate):能有效穿越血腦屏障,增加腦電電壓約 4.7 μV,縮短認知反應延遲。
酸櫻桃汁(Tart Cherry Juice):富含天然褪黑素與花青素。臨床數據顯示每日兩杯可使失眠者增加約84分鐘的總睡眠時間。
番紅花(Saffron)萃取物
機制:番紅花成分(crocin, crocetin)能調節GABA系統,顯著改善入睡延遲並增加深度睡眠。番紅花同時能抑制色胺酸往壓力路徑的分流,讓更多原料用於褪黑激素合成,幫助身體「恢復自然節律」而非從外部強制補充訊號。
臨床:每日攝取 20–30 mg 提取物可有效降低失眠指數(AIS),且其保護認知的能力在某些研究中展現出與藥物相當的潛力。
乳蛋白肽(α-casozepine)與L-茶胺酸
乳蛋白肽:如 Lactium®,能與 GABA_A 受體結合,模擬自然鎮靜效果,幫助增加深度睡眠時長(約+37分鐘)。
L-茶胺酸:茶葉中的核心成分,能增加腦部α波,促進放鬆並優化睡眠維持度。不會讓人昏昏欲睡,而是讓大腦從「高速運轉」過渡到「放鬆清醒」,這個過渡是進入自然睡眠的必要條件。
超越「讓你睡著」:神經新生與 BDNF 的支持策略
前面所說的成分,主要針對「讓你更容易進入深眠」這個目標。
如果你關心的不只是當下的睡眠品質,而是長期的認知健康與大腦可塑性,還需要同時支持神經新生機制和 BDNF 訊號的正常運作。
目前有研究支持的策略:
有氧運動(最強的 BDNF 促進因子):規律有氧運動是目前已知最有效的 BDNF 提升方式,也是促進海馬迴神經新生的最強介入。每週 150 分鐘中等強度有氧,效果在多項研究中被一致確認。
睡眠規律(不只是睡眠時長):神經新生的品質高度依賴睡眠時序的穩定性,而不只是睡了幾個小時。固定的就寢和起床時間,比週末補眠更能維持海馬迴的神經幹細胞活性。
慢性發炎控制:發炎環境會把海馬迴的神經新生從「生長模式」切換到「凋零模式」。 Omega-3、抗氧化植化素、以及避免長期高升糖飲食,都是降低神經發炎的實際手段。
慢性壓力的早期偵測:皮質醇持續偏高是神經新生最直接的抑制因子。這不只是「壓力管理」的問題——它是一個有具體分子路徑的生理問題,需要具體的介入,而不只是放鬆心情。
從今晚開始的選擇
睡眠不是被動的休息,它是大腦最主動的修復時段。
類淋巴系統的清洗、神經新生的維持、BDNF 訊號的正常運作——這些都在你閉上眼睛的那幾個小時裡發生。
而這些能不能順利進行,取決於兩件事:你是否真正進入深度睡眠,以及你的神經系統在睡前是否有足夠的靜默條件。
幾件可以從今晚開始做的事:
睡眠環境:溫度維持在 18–20°C,入睡前 1 小時減少藍光暴露,避免睡前飲酒。
睡眠規律:固定的就寢和起床時間,比任何補眠策略都更重要。
神經系統平靜:如果你的腦袋在睡前停不下來,這是神經系統還沒有退出「備戰狀態」的生理訊號,不是意志力問題。這個節點,是可以被具體介入的。
長期策略:規律有氧運動、慢性發炎控制、壓力累積的早期偵測。這些不只影響睡眠品質,它們直接決定你的大腦在 30 年後的狀態。
👉 想了解如何用針對性的配方幫助神經系統在睡前真正靜下來? 閱讀下一篇:MYND360如何在睡前一小時幫大腦強制關機
延伸閱讀
參考資料
- Fultz, N. E et al., 2019. Coupled electrophysiological, hemodynamic, and cerebrospinal fluid oscillations in human sleep. Science 366(6465):628-631.
- Xie, L et al., 2013. Sleep drives metabolite clearance from the adult brain. Science 342(6156):373-7.
- Chanung Wang, David M Holtzman, 2020. Bidirectional relationship between sleep and Alzheimer’s disease: role of amyloid, tau, and other factors. Neuropsychopharmacology 45(1):104-120.
- Sarah M Rothman, Mark P Mattson, 2012. Sleep disturbances in Alzheimer’s and Parkinson’s diseases. Neuromolecular Med 14(3):194-204.
- Emily Simmonds et al., 2025. Sleep disturbances as risk factors for neurodegeneration later in life. NPJ Dementia 1(6):1-10.
- Qiwei Ji et al., 2025. Global burden of early-onset Parkinson’s disease, 1990-2021: results from the Global Burden of Disease Study 2021. J Neurol Neurosurg Psychiatry. 97(1):33-43.
- Federica Conti, 2025. Dietary Protocols to Promote and Improve Restful Sleep: A Narrative Review. Nutrition Reviews 00(00):1–19.
- Fateme Barforoush et al., 2025. The Effect of Tart Cherry on Sleep Quality and Sleep Disorders: A Systematic Review. Food Sci Nutr. 13(9):e70923.
- Daniel Bricker, Jake Pates, 2025. The Combined Effects of Tart Cherry Powder and Magnesium L-Threonate Supplementation on Cognitive Function and Sleep Architecture: A Pilot Study in Healthy Adults. JCMAH 13(2).
- Schuster, J et al., 2025. Effect of a saffron extract on sleep quality in adults with moderate insomnia. Sleep Med X 10:100147.
- Norouzi, A et al., 2025. Saffron’s promise: a systematic review of its role in Alzheimer’s treatment. Egypt J Neurol 61(21),
- Cotter, J et al.,2026. Examining the effect of L-theanine on sleep: a systematic review. Nutr Neurosci 29(2):224-238.
- Lim, S. E et al., 2024. Dietary supplementation with Lactium and L-theanine alleviates sleep disturbance in adults: a double-blind, randomized, placebo-controlled clinical study. Front Nutr 11:1419978.
- Dagum, P et al., 2025. A wireless device for continuous measurement of brain parenchymal resistance tracks glymphatic function in humans. Nat Biomed Eng. 9(10):1656-1676.
- Disouky A et al., 2026. Human hippocampal neurogenesis in adulthood, ageing and Alzheimer’s disease. Nature 10.1038/s41586-026-10169-4.
- Xin Shi et al., 2026. The protein RAB5IF promotes BDNF signaling by stimulating the SUMOylation of Gαi1/3 to reduce depressive-like behaviors in mice. Science Signaling 19(931)
- Mestre, H., et al., 2018. Flow of cerebrospinal fluid is driven by arterial pulsations and is reduced in hypertension. Nat Commun 9(4878)
- Mortensen, K. N., et al., 2019. Impaired glymphatic transport in spontaneously hypertensive rats. J Neurosci 39(32):6365-6377.
先不要急著補,先看你現在屬於哪一型
如果你最近也有類似的情況,建議先做一個系統化的評估,看看你的身體警報目前在哪個水位。
⚡ 花 1 分鐘做身體警報風險評估評估結果是第一步。完成後,把結果和你的健檢數據一起帶進來,才能看出真正的方向。