牙齦出血不是小事——它是慢性發炎正在擴散到你大腦的訊號
你上一次刷牙,牙齦有沒有出血?
如果有,你大概告訴自己:刷太用力了,或者最近比較累。
然後就沒有然後了。
這是幾乎所有人的反應。牙齦出血太常見,常見到我們認為它不重要。
但 2019 年,一篇發表於《Science Advances》的研究讓口腔健康領域的人都沉默了一下。
研究者在 阿茲海默症患者的大腦切片裡,找到了牙周病的主要致病菌——牙齦卟啉單胞菌(Porphyromonas gingivalis)。
不只找到了細菌,還找到了它分泌的毒素——牙齦蛋白酶(Gingipain)——直接沉積在神經組織裡。
牙菌斑裡的東西,跑進了大腦。
它是怎麼進去的
口腔和大腦,看起來距離很遠。
但 2024 - 2025 年的研究確認,牙周病菌進入大腦有 兩條路徑,不只是一條。
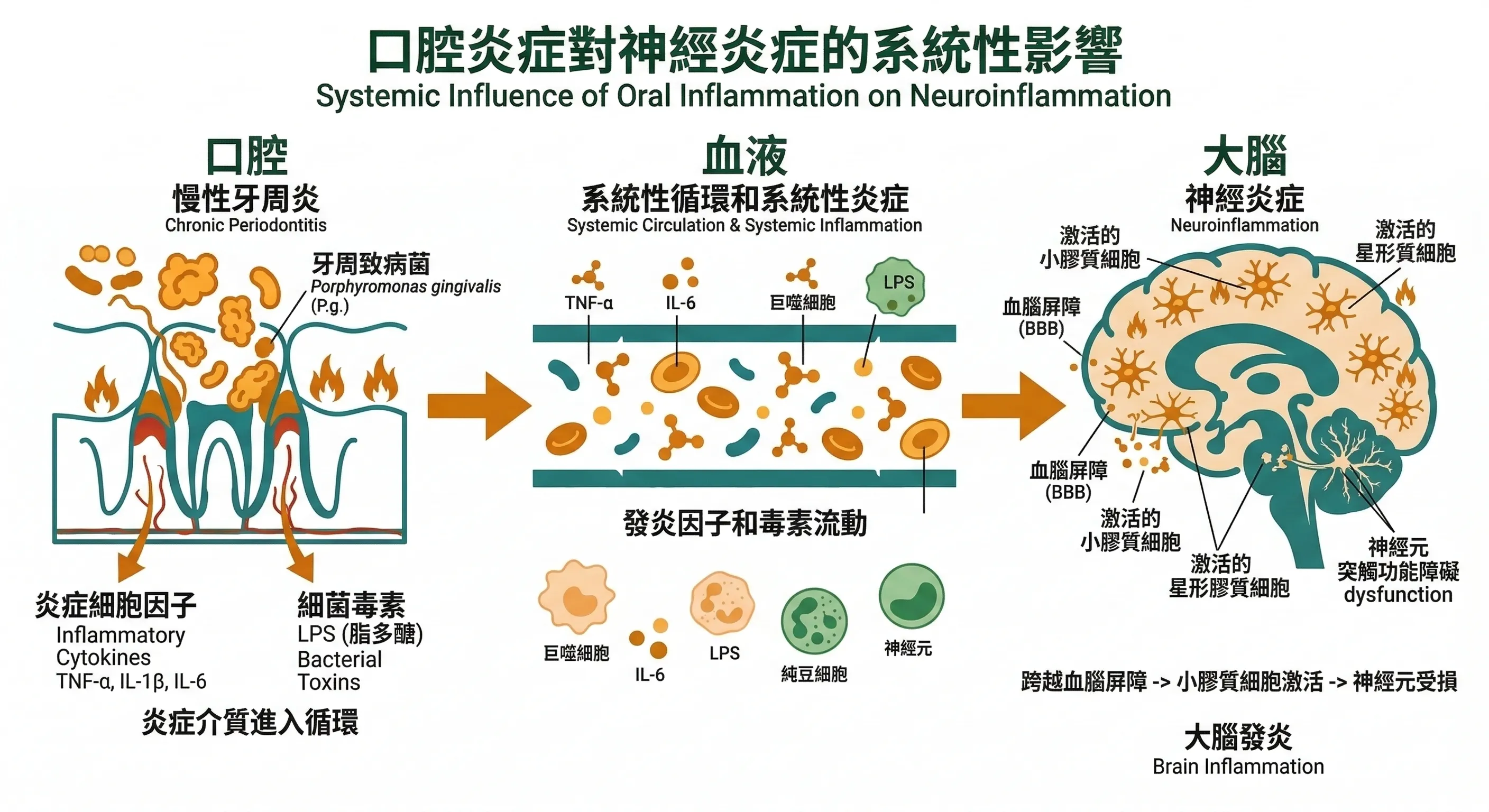
第一條:血液循環(菌血症)——當牙周組織反覆發炎,牙齦屏障被破壞,細菌就有機會進入血液循環——這個現象叫做菌血症(Bacteremia),程度輕微時你完全感覺不到,但它每天都可能發生:刷牙、用牙線、甚至咀嚼食物的時候。
P. gingivalis 進入血流後,其毒素 牙齦蛋白酶(Gingipain) 會破壞血腦屏障的通透性,讓細菌和發炎物質得以滲入腦組織。
第二條:神經路徑(三叉神經 / 嗅神經)——這是比菌血症更直接的路徑。
P. gingivalis 產生的外膜囊泡(OMVs)能沿著三叉神經或嗅神經的軸突,不經過血液直接進入中樞神經系統——就像一輛不走高速公路、走山路直達的車。
這兩條路徑加在一起,解釋了為什麼 100% 有心血管疾病的患者冠狀動脈中都能找到 P. gingivalis——這種菌的全身擴散能力,遠比一般人以為的強。
進入大腦之後,發生了什麼?
P. gingivalis 觸發 兩個阿茲海默症的核心病理:
一是促進 類澱粉蛋白(Aβ)斑塊沉積——這是阿茲海默症最經典的病理標誌,長期以來是藥物研發的主要靶點。
二是觸發 tau 蛋白過度磷酸化,形成神經纖維纏結(neurofibrillary tangles)——這是阿茲海默症的第二個核心病理標誌,與認知衰退的速度直接相關。
同時,大腦裡的免疫細胞 微膠細胞(Microglia) 被持續激活,進入慢性過度激活狀態,開始分泌過量的神經毒性物質,神經元開始凋亡。
認知功能,開始下滑。
數字說明了什麼
研究不只有一篇。這條「口腔-大腦」的發炎路徑,過去二十年累積了越來越清晰的證據。
牙周病診斷後十年內,失智症風險加倍: 多項前瞻性研究的綜合分析顯示,牙周病患者在確診後十年內,發展出阿茲海默症的風險是無牙周病者的 兩倍。這個數字與吸菸、糖尿病等已確立的失智症危險因子屬同一量級。
缺牙和失智症的直接關聯: 2012 年,日本神奈川齒科大學的研究追蹤了 4,425 位 65 歲以上長者四年,結果發現:牙齒少於 20 顆且沒有裝假牙的人,罹患失智症的風險是牙齒健全者的近 2 倍。
阿茲海默症患者的牙齒狀況: 名古屋大學的研究比較了健康老人與阿茲海默症患者的口腔狀況,發現病患平均只有健康老人 1/3 的牙齒,而且比健康老人早了 20 年開始掉牙。
咀嚼能力與認知衰退: 2020 年《Aging》期刊一份追蹤 22 年、554 位受試者的研究發現:咀嚼能力的下降程度,與智力衰退的速度 呈正相關。
這些數字描述的不是「缺牙比較不方便」。
它們描述的是:口腔的健康狀態,影響著大腦老化的速度。
牙周病為什麼這麼普遍卻這麼被忽略
台灣成人牙周病盛行率超過 90%,但大多數人不知道自己有牙周病。
原因很簡單:牙周病的早期幾乎 完全沒有疼痛感。
牙齦出血、輕微腫脹、偶爾口臭——這些「太常見」的症狀,我們習慣了就忽視。
但這就是牙周病在進展的訊號,也是慢性發炎正在擴散的訊號。
牙周病的致病機制很清楚:口腔細菌形成 牙菌斑,長期刺激牙齦,引發局部發炎反應。
如果沒有處理,發炎深入牙周韌帶和齒槽骨,破壞支撐牙齒的結構,最終導致牙齒鬆動和脫落。
但在這整個過程中,發炎反應不只停在牙齦。
它同步在血液裡擴散,同步在全身的器官裡製造損傷。
這和你整體的老化速度有什麼關係
這裡需要引入一個比較大的框架。
老化研究在過去二十年裡建立了一個核心概念:Inflammaging——老化本身就是一種慢性低度的全身性發炎狀態。
幾乎所有最常見的老化相關疾病——心血管疾病、第二型糖尿病、阿茲海默症、肌肉流失——背後都有這個共同的發炎底火在燒。
牙周病,在這個框架裡是什麼?
它是 讓發炎底火持續加料的一個輸入來源。
每一次刷牙時牙齦出血,每一次咀嚼時細菌入血,都是在讓那個底火再燒旺一點。
這不是今天感覺得到的事,但它在十年、二十年的時間軸上,確實在改變你的生理老化速度。
這就是為什麼口腔健康不只是牙科問題。
你現在可以做的事
不需要等到缺牙才開始處理,而且現在有臨床數據說明早點處理是有效的。
2025 年紐約大學(NYU)發表於《Neuroepidemiology》的一項 12 年前瞻性世代研究追蹤了 866 位有牙周症狀的老年人。
結果發現:有接受牙周治療的人,失智症發病率比沒有治療的人低了 38%,認知功能的年度下降速度也顯著較慢。
這個效果在不同性別、種族和教育程度的受試者中都一致。
另一項德國的研究(Schwahn et al.)對 177 位牙周治療患者進行了長達 7 年以上的腦部影像追蹤,發現接受牙周治療者的阿茲海默症相關腦萎縮程度,相當於從第 50 百分位下降到第 37 百分位——意即牙周治療實際上延緩了大腦老化。
這些數字說的是:定期洗牙和牙周治療,不只是牙科保健,而是有臨床根據的失智症預防策略。
定期洗牙(每半年一次) 是目前最有效的牙周病預防手段。
健保給付 12 歲以上每半年一次,有牙周病或特殊疾病的患者可與牙醫師討論是否需要縮短至每三個月。這不是選配,是底線。
刷牙的核心任務:破壞牙菌斑生物膜。 牙刷能清潔的範圍大約只有牙齒表面的 60%,剩下 40% 藏在牙縫裡。
牙縫裡的厭氧菌在分解蛋白質的過程中會產生揮發性硫化物,這是口臭的化學來源,也是牙周發炎持續進行的場域。
清除它的方式只有一種:物理摩擦。
牙線不是用來挖食物殘渣的,是用來刮除牙縫生物膜的。 正確做法是讓牙線貼著牙齒表面上下刮動,而不是在牙縫裡「拉鋸」。
漱口水是物理清潔之後的化學輔助,如果生物膜還完整黏附在牙齒上,抗菌藥水根本滲透不進去——清潔順序不能顛倒。
刷牙頻率的優先順序:睡前那次是絕對不能妥協的。 睡覺時唾液分泌大幅減少,口腔失去天然的沖刷機制,是細菌活動最旺盛的時段。
如果牙縫裡帶著三餐殘留物入睡,等於讓細菌在最理想的環境裡持續產酸、持續發炎整整八小時。
一天只能做一次的話,就做睡前這次,並且做確實——每一面都刮到,不要圖快。
牙縫較大或有牙周病史的人,牙間刷 的效率高於牙線,選擇「剛好能進入但不費力」的尺寸是關鍵;牙縫緊密的人用標準牙線即可,不要強行使用牙間刷。
沖牙機 是輔助工具,無法取代牙線或牙間刷的物理刮除功能。
但更根本的問題是:口腔的慢性發炎只是全身性 Inflammaging 的一個切面。
如果你的整體發炎狀態沒有被管理,處理口腔只是局部處理,不是解決問題的全部。
接下來讀這篇:
抗慢性發炎就是在抗老化——這不是廣告詞,這是2000年就確立的科學
還不確定自己的身體目前累積了多少慢性發炎?
參考資料
- Dominy SS et al., 2019. Porphyromonas gingivalis in Alzheimer’s disease brains: Evidence for disease causation and treatment with small-molecule inhibitors. Science Advances. 5(1):eaau3333.
- Yamamoto T et al., 2012. Dental status and incident falls in older Japanese adults: A prospective cohort study. Psychosom Med. 74(4):385-391.
- Ando Y et al., 2020. Masticatory function and cognitive decline in the elderly: A 22-year follow-up study. Aging (Albany NY). 12(4):3080-3092.
- Ide M et al., 2016. Periodontitis and cognitive decline in Alzheimer’s disease. PLoS One. 11(3):e0151081.
- Franceschi C, Campisi J, 2014. Chronic inflammation (inflammaging) and its potential contribution to age-associated diseases. J Gerontol A Biol Sci Med Sci. 69 Suppl 1:S4-9.
- Kamer AR et al., 2008. Alzheimer’s disease and peripheral infections: The possible contribution from periodontal infections, model and hypothesis. J Alzheimers Dis. 13(4):437-449.
- Qi X et al., 2025. Association of gum treatment with cognitive decline and dementia risk among older adults with periodontal symptoms: a 12-year prospective cohort study. Neuroepidemiology. 59(4):313-322.
- Schwahn C et al., 2022. Effect of periodontal treatment on preclinical Alzheimer’s disease. Alzheimer’s & Dementia. 18(7):1175-1185.
- Jiang Y et al., 2025. Porphyromonas gingivalis-induced periodontitis promotes neuroinflammation and neuronal loss associated with dysfunction of the brain barrier. Front Cell Infect Microbiol. 15:1559182.
- Liu S et al., 2024. Porphyromonas gingivalis and the pathogenesis of Alzheimer’s disease. Crit Rev Microbiol. 50(2):127-137.
- Cho HA et al., 2024. Association of periodontal disease treatment with mortality in patients with dementia: a population-based retrospective cohort study. Sci Rep. 14:5243.
先不要急著補,先看你現在屬於哪一型
如果你最近也有類似的情況,建議先做一個系統化的評估,看看你的身體警報目前在哪個水位。
⚡ 花 1 分鐘做身體警報風險評估評估結果是第一步。完成後,把結果和你的健檢數據一起帶進來,才能看出真正的方向。